Описание
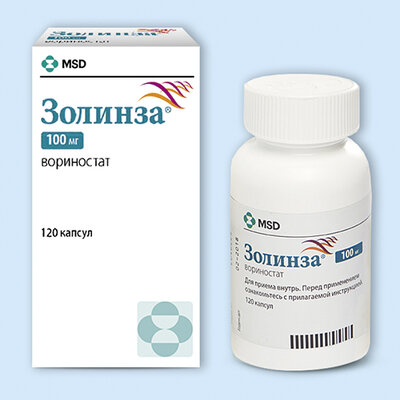
Препарат Золинза — это современное противоопухолевое средство, которое используется при прогрессирующей или стойкой первичной кожной Т-клеточной лимфомы, а также при рецидиве после предыдущих системных курсов противоопухолевого лечения. Основное действующее вещество препарата — вориностат.
Эффективность препарата Золинза исследовалась у больных с кожной формы Т-клеточной лимфомы во IIB стадии и выше. Объективный эффект зарегистрирован у 30% пациентов, всего на терапию данным препаратом ответило 46% пациентов. Некоторые визуальные улучшения отмечались у 77 процентов пациентов. У пациентов, страдающих от нестерпимого зуда, также отмечалась положительная динамика.
Показания препарата Золинза
- лечение кожной Т-клеточной лимфомы, несмотря на проведенную системную терапию, которая прогрессирует, рецидивирует или персистирует.
Состав Золинза
- Активное вещество: вориностат 100,0 мг
- Вспомогательные вещества: целлюлоза микрокристаллическая, кроскармеллоза натрия, магния стеарат.
- Оболочка капсулы: титана диоксид (Е171), желатин.
- Чернила: Опакод черный (Opacode Black) S-l-17822: шеллака глазури раствор в этаноле, краситель железа оксид черный, бутанол, изопропанол, пропиленгликоль, аммония гидроксид. Или Опакод черный (Opacode Black) S-1-17823: шеллака глазури раствор в этаноле, краситель железа оксид черный, бутанол, изопропанол, пропиленгликоль, аммония гидроксид.
Фармакологическое действие
Вещество вориностат — сильный ингибитор гистон-деацетилаз (HDAC) — HDAC1, HDAC2 и HDAC3, а также HDAC6. Эти ферменты катализируют отщепление от лизиновых остатков белков ацетиловой группы, в т.ч. белков-факторов транскрипции и гистонов. Противоопухолевое свойство вориностата связано с ингибированием активности HDAC с дальнейшим накоплением ацетилированных белков, включая гистоны. Ацетилирование гистонов сопровождается транскрипционной активацией генов, в т.ч. генов-супрессоров опухолей, а их экспрессия, в свою очередь, индуцирует апоптоз клеток или дифференцировку и подавление опухолевого роста клеток. Концентрация вориностата, вызывающая накопление ацетилированных гистонов, также обусловливает ингибирование клеточного цикла, апоптоз или дифференцировку видоизмененных клеток.
Вориностат по данным исследований на клеточных культурах индуцирует апоптоз у большого числа видоизмененных (опухолевых) клеток. Вориностат на культурах опухолевых клеток при совместном использовании с другими видами противоопухолевой терапии показал дополнительную или синергичную активность, включая лучевую терапию и химиотерапию цитотоксическими препаратами, индукторами дифференцировки клеток, ингибиторами киназ. Вориностат in vivo, на широком диапазоне моделей рака у грызунов, включая модели ксенотрансплантатов злокачественных опухолей молочной железы, толстой кишки, простаты человека показал противоопухолевую активность.
Фармакокинетика
Всасывание
При однократном приеме внутрь вориностата в дозировке 400 мг одновременно с жирной пищей у больных с рефрактерными или рецидивирующими распространенными опухолями средние значения ± стандартное отклонение AUC, Cmax и медианы (диапазона) Tmax составили 5.5±1.8 мкмоль/л×ч, 1.2±0.62 мкмоль/л и 4 (2-10) ч соответственно. При однократном приеме внутрь препарата Золинза в дозиовке 400 мг натощак средние значения AUC, Cmax и медианы Тmах составили 4.2±1.9 мкмоль/л×ч, 1.2±0.35 мкмоль/л и 1.5 (0.5-10) ч соответственно. Одновременный прием вориностата, таким образом, с жирной пищей сопровождается повышением (на 33процента) всасывания и незначительным снижением скорости всасывания (задержка наступления Тmах на 2.5 часа) в сравнении с приемом препарата Золинза натощак. Предполагается, что отклонения фармакокинетических параметров незначительны и не имеют клинического значения.
После многократного приема внутрь вориностата в дозировке 400 мг одновременно с пищей значения Cmax, медианы Тmах, AUC в равновесном состоянии составили 6.0±2.0 мкмоль/л×ч, 1.2±0.53 мкмоль/л и 4 (0.5-14) ч соответственно.
Распределение Золинза
Связывание вориностата с белками плазмы в диапазоне плазменных концентраций от 0.5 до 50 мкг/мл составляет примерно 71процент. Препарат Золинза быстро проникает через плацентарный барьер у кроликов и крыс при введении в суточных дозировках 150 мг/кг и 15 мг/кг соответственно (что соответствует меньшему значению экспозиции, чем у человека по данным AUC0-24). Примерно через 30 мин после введения достигается трансплацентарное равновесие.
Метаболизм
Реакции глюкуронизации и гидролиза с последующим β-окислением являются основными путями метаболизма препарата Золинза. плазменные концентрации двух метаболитов — О-глюкуронида вориностата и 4-анилино-4-оксобутановой кислоты были измерены. Оба метаболита фармакологически неактивны. В равновесном состоянии экспозиция О-глюкуронида вориностата и 4-анилино-4-оксобутановой кислоты в сыворотке крови превышает экспозицию вориностата примерно в 4 и 13 раз соответственно, по сравнению с вориностатом.
In vitro проведенные исследования на микросомах печени человека указывают на незначительную биотрансформацию препарата Золинза ферментами системы цитохрома Р450.
Выведение Золинза
Вориностат преимущественно метаболизируется в печени. Почками выводится в неизмененном виде менее 1% введенной дозы. Таким образом, почечная экскреция на выведение препарата из организма практически не влияет. В моче при достижении равновесного состояния обнаруживали два фармакологически неактивных метаболита вориностата — 4-анилино-4-оксобутановую кислоту в количестве 36±8.6% от введенной дозы вориностата и О-глюкуронид вориностата в количестве 16±5.8% от введенной дозы вориностата. количество обнаруживаемых? таким образом, в моче неизмененного вориностата и двух указанных метаболитов составило в среднем 52±13.3% от принятой дозы вориностата. период полувыведения препарата Золинза и О-глюкуронида составил около 2 часов, а период полувыведения 4-анилино-4-оксобутановой кислоты — примерно 11 часов.
Фармакокинетика у особых групп пациентов
Пол, раса и возраст пациентов, по данным анализа ограниченного объема данных, клинически значимого влияния на фармакокинетические параметры вориностата не оказывали.
Дети.
У детей и подростков до 18 лет фармакокинетические параметры вориностата не изучены.
Пациенты с печеночной недостаточностью.
Вориностат противопоказан к использованию у больных с печеночной недостаточностью тяжелой степени. Препарат Золинза необходимо применять с осторожностью у больных с печеночной недостаточностью легкой и средней степени. Эти рекомендации основаны на данных фармакокинетических исследований. Согласно этим исследованим предполагается, что после приема вориностата риск дозозависимой токсичности выше, у пациентов с тяжелой степенью печеночной недостаточности, чем у пациентов без нарушений функции печени, даже при приеме сниженной дозировки препарата Золинза. Суточная переносимая доза вориностата для больных с легкой и средней степенью печеночной недостаточности составляет 300 мг и 200 мг.
Пациентов с тяжелой степенью печеночной недостаточности из исследования вориностата исключили. Есть ограниченное число больных с печеночной недостаточностью средней степени, которых включили в клинические исследования. клинически значимого различия в развитии побочных эффектов, связанных с функцией печени, не обнаружено, у пациентов с печеночными нарушениями в анамнезе по сравнению с пациентами без таковых.
Пациенты с почечной недостаточностью.
У пациентов с почечной недостаточностью не изучены фармакокинетические параметры препарата. почечная экскреция, следует отметить, не влияет на элиминацию вориностата из организма.
Фармацевтические характеристики Золинза
Капсулы твердые желатиновые, размер №3, непрозрачные, белого цвета, с черной надписью «568» и белой надписью на черном фоне «100 mg». Содержимое капсул — порошок от белого до светло-оранжевого цвета.
Упаковка, срок годности, условия хранения Золинза
По 120 капсул во флаконе. Флакон — из полиэтилена высокой плотности, запаянный защитной мембраной и закрытый пластмассовой крышкой с устройством против вскрытия флакона детьми.
Вместе с инструкцией по применению по одному флакону в картонную пачку.
Препарат Золинза следует хранить в недоступном для детей месте при температуре не выше 30°С.
Срок годности — 3 года. Не использовать по истечении срока годности, указанного на упаковке.
Особые указания
Контакта содержимого капсулы с кожей и слизистыми оболочками следует избегать. При контакте тщательно смыть порошок водой.
Наша компания работает как на территории Казахстана, так и осуществляет доставку в страны ближнего зарубежья. Обращайтесь к нам за консультациями по контактным телефонам.